2, 3-difosfoglyceratet (2, 3 DPG) är en förening härledd från en mellanprodukt av glykolys; Det koncentrerar sig särskilt på erytrocytnivån, eftersom de röda blodkropparna saknar mitokondrier - utnyttjar den anaeroba laktatmetabolismen (homolaktisk fermentering av glukos) för att erhålla energi.
Hemoglobin är ett tetrameriskt protein, som bildas av fyra underenheter, två alfa och två beta, var och en består av en proteindel (globin) och en EME (protesgrupp som binder syre). 2, 3-difosfoglycerat fäster till Betakedjor genom komprimering av dem och reducering av hemoglobins affinitet för syre.
Bindningen av 2, 3 DPG till hemoglobin uppträder när den är i den deoxifierade formen, medan den är upplöst i lungan från bindningen av hemoglobin till syre. I själva verket när hemoglobinet når vävnaderna är p-kedjorna de första som ger upp syret och denna förlust involverar en förskjutning av monomererna från mitten. När den inre hydrofila håligheten öppnar kommer DPG in i och binder till de tetramerbildande heteropolära bindningarna mellan dess negativt laddade grupper och lysin- och histidinresterna av beta-kedjorna, positivt laddade. Den sålunda stabiliserade strukturen kan också frigöra syre av de två a-kedjorna. I lungorna sker emellertid omvänd process. vid högt syretryck är a-kedjorna de första som binder den och DPG "squeezes" och utvisas från tetrameren, vilket möjliggör en enklare syre-kedj-p-bindning.
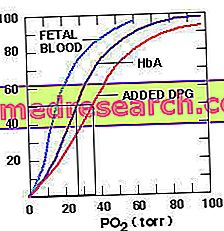
2, 3-bisfosfoglyceratet kan inte binda till fetalt hemoglobin, eftersom denna molekyl saknar B-kedjorna med vilka 2, 3 DPG drar sin länk. Detta förklarar den högre affiniteten för syre i fetalt hemoglobin jämfört med moderns hemoglobin, en egenskap som gör det möjligt för fetalt blod att extrahera syre från moderns blod.



